低温環境の利用技術 | 19
過冷却現象の基礎とその利用技術
2025年8月28日
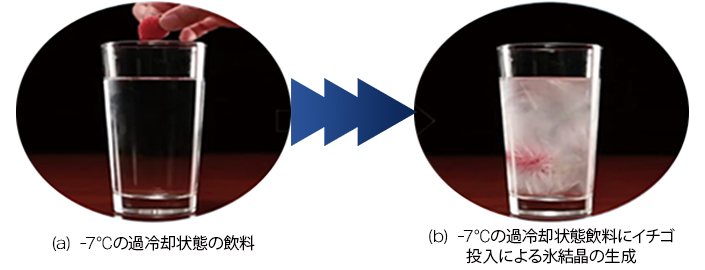
写真1 過冷却状態の飲料にイチゴを落とした場合のシャーベット状氷生成8)
写真1は、(a)冷凍庫内で過冷却状態にした飲料(-7℃)に、過冷却状態解消にイチゴを投下することで、写真(b)に見られるようなシャーベット状の氷結晶が生成されます。
各種のジュース、炭酸水、コーヒーやアルコール飲料など水分を含む飲料の過冷却状態を利用することで、スラリー状やシャーベット状の氷結晶の生成が可能です。
過冷却状態の飲料から様々な氷結晶生成のメカニズムについては、後述の(2)過冷却状態の利用における項目(d)において説明します。
第19回サイエンスコラムの連載は、水などの過冷却現象の基礎とその利用技術に関して解説します。
(1)過冷却現象の基礎
一般に液体をその凝固温度(平衡凍結温度)以下に冷却しても、液体は凍結せずに液体状態を維持します。この状態を過冷却(supercoolingまたはundercooling)現象と呼び、不安定な液相状態です。この過冷却状態は、自然界などにおいて多く観察される現象です。例えば、雲は微細な過冷却状態の水滴などから構成されており、その微細水滴は-20℃程度になっても過冷却状態を維持します。さらに、直径数µm程度の微細な水滴は、-40℃近くまで過冷却状態を維持するとの実験結果も報告されています。さらに、比較的大きな過冷却水滴群が道路などに落下し、その衝撃で過冷却状態が解消されて、道路面が滑らかな氷層で覆われて、交通障害を引き起こすことが知られています。この現象はフリージングレインと呼ばれており、寒冷地の北米などで報告されています。また、第3回サイエンスコラム「水道管の凍結メカニズムとその利用」(2)において解説しましたように、水道管内で静止している水道水が寒冷下で過冷却水の状態から凍結が進行し、樹枝状氷結晶群が水道管内を閉塞する、いわゆる水道管の凍結事故があります。このように、過冷却現象は、自然界や産業界などで多く見られます。
以下に、過冷却の発生機構を解説し、さらにその制御方法についても解説します。
(a)凍結と融解現象および過冷却解消と安定化機構
分子レベルにおけるミクロ現象の立場からは、凍結界面の状態は液相側の水分子が相変化(液体→固体)を伴いながら固相(氷)界面に、ある凍結速度\(V_f\)で組み込まれます。一方、界面上の固相分子は相変化(固体→液体)を伴って、ある融解速度\(V_m\)で液相側へ拡散します。
図1は、温度\(T\)に対する凍結速度\(V_f\)と融解速度\(V_m\)の関係を示したもので、両方の速度が同一となる(\(V_f=V_m\))温度が平衡凍結温度\(T_e\)です。\(T_e\)付近では固液界面の分子・原子活性化エネルギーと幾何学的配置および分子原子の収容能力の差により、\(V_m\)が\(V_f\)よりも急激に立ち上がることになります1)。
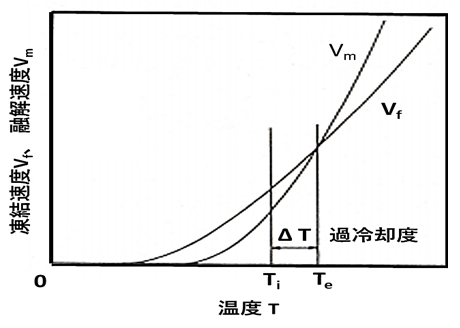
図1 凍結速度\(V_f\)と融解速度\(V_m\)の温度依存性
図1に示す温度領域\(T \lt T_e\)では、凍結速度\(V_f\)が融解速度\(V_m\)を上回り、凍結界面の進行がみられることになります。真の凍結速度\(V\)は(\(V_f-V_m\))であり、図2に示すように、真の速度\(V\)の最大値が存在することになります。より低い温度\(T_i\)で\(V=0\)となるのは超急速冷却により非結晶(アモルファス)の凝固組織となるためです。図中の\(ΔT\)は、平衡凍結温度\(T_e\)と過冷却水温度\(T_i\)の温度差(\(T_e-T_i\))で過冷却度(degree of supercooling)を意味します。水分子の氷結晶への相変化は、潜熱エネルギーの放出にて起こるもので、凍結界面における熱収支の程度が、その凍結速度そして氷結晶の状態を規定する一つの重要な因子となります。
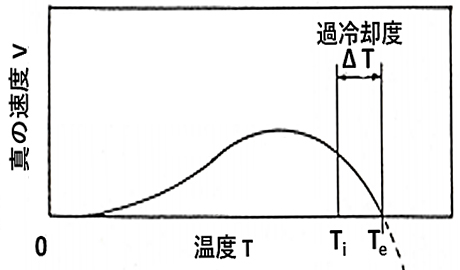
図2 真の凍結速度Vの温度依存性
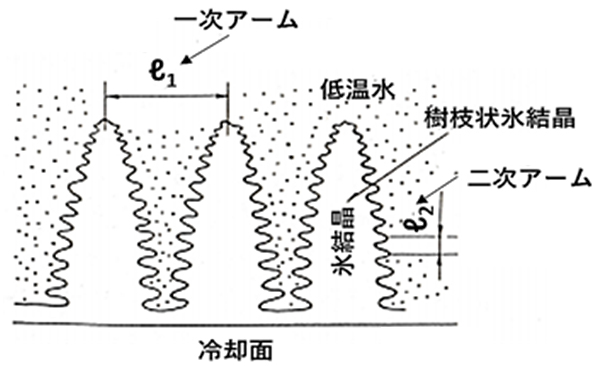
写真2(左側)および図3(右側)は、過冷却水の下面からの冷却で形成される樹枝状氷結晶の可視化写真(過冷却度\(ΔT=0.607\)K)および結晶成長の模型を示したものです。写真2の右側は樹枝状氷結晶を正面から撮影したもので、左側は側面で先細りの板状構造が観察されます。これらの樹枝状氷の成長形態を図3の模型図に基づいて説明すると、まず樹枝状氷の幹となる一次アームが間隔\(ℓ_1\)で冷却面より過冷却水中へ成長します。その後、一次アーム方向と垂直方向に緻密な間隔\(ℓ_2\)を持つ二次アームが形成され、樹枝状氷結晶構造が完成します。
このような樹枝状結晶の先端部の形状とその成長速度\(u\)は、図4に示す樹枝状氷結晶先端部の成長モデルにより説明することができます。図4に示すように、結晶先端部の氷結晶成長過程では、界面近傍の過冷却水相の温度勾配は大きく、相変化に伴う潜熱の拡散が容易となり、氷結晶の成長を助長する力となります。一方、氷結晶界面の張力は、同界面曲率\(r\)と平衡温度\(T_e\)の関係(ギブス・トムソン効果*1)により突出部の融点を下げることになります。 すなわち、突出部を元に戻そうとする力として働くことになります。
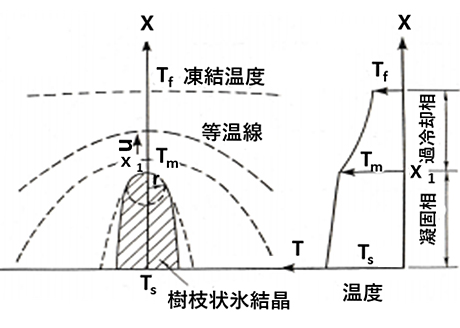
図4 樹枝状結晶先端の成長モデル
図5は、凝固温度以下のある温度Tにおける過冷却度\(ΔT(=T_e-T)\)に対する結晶成長速度\(u\)と結晶曲率半径\(r\)の定性的関係を示したものです。曲率半径\(r\)が小さいとギブス・トムソン効果により融点\(T_m\)が下がり、結晶成長速度\(u\)が小さくなります。一方、極端に曲率\(r\)が大きくなると界面よりの潜熱の拡散が小さくなり、成長速度も小さくなります。結果として、先端の結晶成長速度\(u\)の最大となる曲率半径が存在することになります。樹枝状氷結晶の成長速度は、\(u=10~15\)µm/s程度とされています。
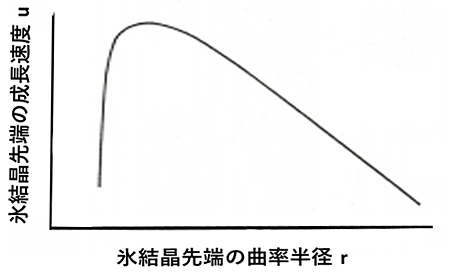
図5 結晶先端の曲率半径\(r\)とその成長速度\(u\)の関係
*1:ギブス・トムソン効果:結晶の界面が曲率を持つと界面の曲率に比例して局所的な融点が変化する現象です。
図6は、バルク状態(物質の界面に触れていない、内側の部分の状態)の不純物を含まない水を徐冷した場合における水と氷温度の経時変化を示したものです。平衡凍結温度\(T_e\)以下の過冷却度\(ΔT_1\)の時点(時間\(t=t_1\))において、氷結晶核の形成が起こり、凍結が始まると、その潜熱放出のために水の温度降下割合が減少します。この時点では冷却速度の方が、凍結による潜熱放出速度よりも大きいために、水側の過冷却度は増大します。さらに時間の経過とともに、凍結界面の面積が増大するにつれ、潜熱放出量も増大し、冷却速度と潜熱放出速度か釣り合った時点で最大過冷却度\(ΔT_{ max }\)となります。その後、潜熱放出速度が冷却速度を上回り、水の温度が上昇に転じます。また、増大した固相(氷)表面で干渉が起こり、潜熱放出速度および\(ΔT\)の減少とともに凍結速度が減少します。さらに、時間\(t_3\)より、\(ΔT_2\) 一定の小さな過冷却度で凍結が進行し、最終的に時間\(t_4\)の時点で凍結が完了することになります。このような過冷却現象を伴う凍結は、潜熱の放出と冷却速度との関係で複雑な様相を呈することになります。
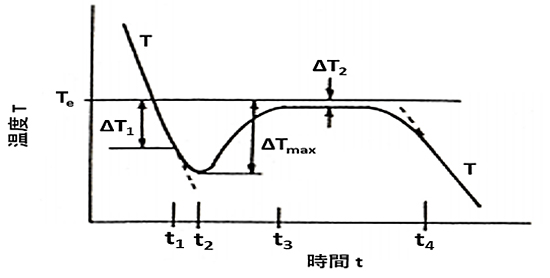
図6 冷却水および氷温度の経時変化
過冷却水からの氷結晶への相変化は氷結晶核の生成に起因するものです。バルク状態の水中の水分子(H2O)は、それぞれ独立にH2Oの分子状態で存在するのではなく、図7に示されるように、水素結合により複数個のH2O分子が結びついた形のクラスターと称する塊を構成単位として振舞っています。温度の低下すなわち過冷却度\(ΔT\)の増大とともに、クラスターを構成する水分子の数も増え、そのクラスターの大きさ(クラスター径)も大きくなります。クラスターを構成する水分子は、水素結合による拘束そして温度低下に伴う粘性(分子間力)の増大により、水とも氷とも言えない状態となります。さらに、その水分子の原子配列も氷結晶に近い六方晶配置に近づき、あるクラスターの限界大きさを越えると氷結晶核となります。このような状態での氷結晶の発生を「均質氷核生成」と呼んでいます。当然のことながら、水分子の集合体となったクラスターの成長は、その周囲の水分子との間に生じた界面エネルギー(表面張力)により、氷結晶の成長が抑制されることになります。
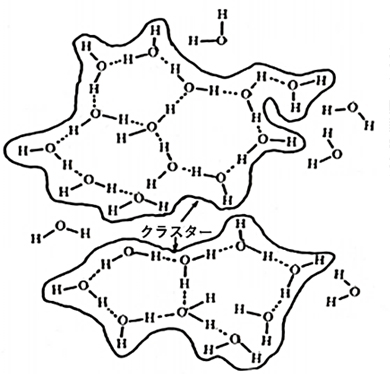
図7 水分子のクラスター構造
(b)氷結晶の成長メカニズムについて
図8に示すように自由エネルギーと温度の関係は、それぞれの相状態で一定の傾きをもった直線で表され、また各相の直線が交差する点が沸点あるいは凝固点の相変態温度に対応します。なお、図中の破線は、過冷却状態における自由エネルギーを示します。一定温度における相変化による自由エネルギーの変化量\(ΔG\)は、\(ΔG=ΔE\)(内部エネルギー)-\(TΔS\)(エントロピーの変化)のように表されます。過冷却水中の前述の水分子クラスターに水分子が1個組み込まれる場合を考えると、固液相間の内部エネルギー差\(ΔE\)は、水分子1個当たりの凝固の潜熱\(L\)に対応するものであり、またエントロピー変化\(ΔS\)は、凝固点温度\(T_e\)において固液相間の平衡が成り立つ(\(ΔG=0\))ことから、\(ΔS=L/T_e\)と表されます。これにより、水分子クラスターに1個の水分子が新たに組み込まれた場合の体積自由エネルギー変化\(Δ\mu \)(過冷却液相と固相の化学ポテンシャルの差)は、\(Δ\mu =LΔT\)(過冷却度)\(/T_e\)となります。一般に水分子クラスターの大きさは非常に小さい(約1~10nm)ことから、その体積に対する表面積の比は非常に大きなものとなり、水分子クラスターと過冷却水の界面に働く界面エネルギー\(σ_{ ct }\)が水分子クラスターの成長を抑制することになります。
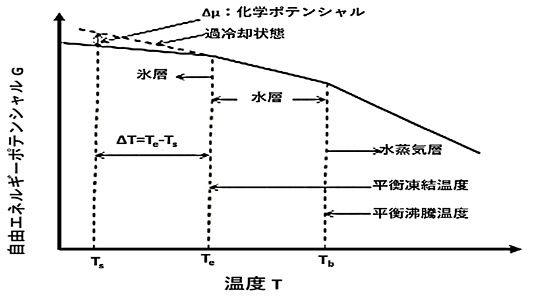
図8 物質の自由エネルギーと温度の関係
半径\(r\)の水分子クラスターに対して液相・固相変化に伴う正味の自由エネルギー変化は、\(\Delta G_{t→c}=4πr^2σ_{ct}-4/3π^3ρ_{c}\Delta μ\)となります。この式で\(ΔG_{ t→c }\)が最大となるのは、関係式を微分することで、\(r^*=2σ_{ct}/\Delta μ\)、\(\Delta G_{ l→s }^*=16πσ_{ ct }^3/(3\Delta μ^2)\)となります。これら得られた値は、図9に示しています。水分子クラスターの大きさが、臨界半径\(r^*\)を超えたときに、その自由エネルギー障壁\(ΔG^*_{ t→c }\)を乗り越えて過冷却水中に氷結晶核が生成され、一旦この臨界半径を越えると、その後組み込まれる水分子はその系の自由エネルギーを一方的に減少させるので、水分子クラスターは急速に巨視的な氷結晶に成長します。
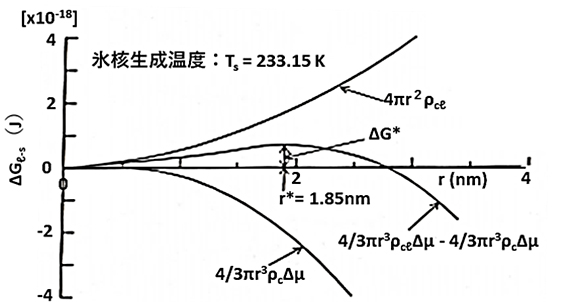
図9 自由エネルギー変化\(ΔG_{ t-c }\)と水分子クラスター半径\(r\)の関係
ここで、水分子クラスターの発生にボルツマン定数、水分子の活性化エネルギーによる氷核生成頻度などを用いることで、過冷却度\(ΔT\)と過冷却液滴の直径\(d_w\)の関係を示したものが図10です。凝固温度以下の温度Tにおける水の過冷却度\(ΔT(=T_e-T)\)は、液滴直径\(d_w\)の増加(体積の増加)に従い緩やかに減少して、その値は30K~40Kの間にあることが理解できます。
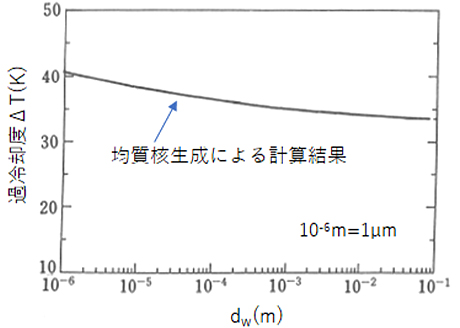
写真10 過冷却度\(ΔT\)と過冷却液滴直径\(dw\)の関係
上述のように「均質氷核生成」水分子のクラスターがある臨界半径を超えた場合に、氷結晶が成長しますが、水道水などの通常の水には数多くの微細な異質浮遊物質が含まれています。このような異質浮遊物質表面上より、異物質による氷結晶の生成が一般的です。このような異質浮遊物質表面から氷核生成する場合を「不均質氷核生成」と呼んでいます。図11は、平均冷却速度\(u_{ cm }=0.4\)K/minの条件にて、それぞれ試料水体積\(V=1\)cm3、 ガラス管内径\(d_i=9.6\)mmにおける純水(電気抵抗\(R=5\times 10^6 \)Ω・cm)および水道水(\(R=2\times 10^4\)Ω・cm)に対する限界過冷却度の平均値\(ΔT_{ wm }\)と異質浮遊粒子径\(R_s\)(µm)の関係を計算結果と実測値を示したものです。図11中の点は、試料水内に含まれる最大の異質浮遊粒子径に対するものであり、その値はフィルター直径\(\phi \)より、\(β=\phi /2\)としています。また、図中それぞれの実線は、水分子クラスターと異質浮遊粒子間の接触角\(\phi \)の大きさを表す表面パラメータ\(β(=cos\phi )\)を種々の値に変化させた計算結果です。限界過冷却度\(ΔT_{ max }\)の実測値は、異質浮遊粒子半径\(R_s\)の低下とともに増加する傾向にあり、その増加割合は、\(R_s=0.1\)µm以下の領域において急激なものとなっています。また、同一の異質浮遊粒子径\(R_s\)においては、純水および水道水に関わらずほぼ同程度の\(ΔT_{ wm }\)となっています。なお、計算結果から実測値の表面パラメータ\(β\)は、0.4~0.6の間にあります。
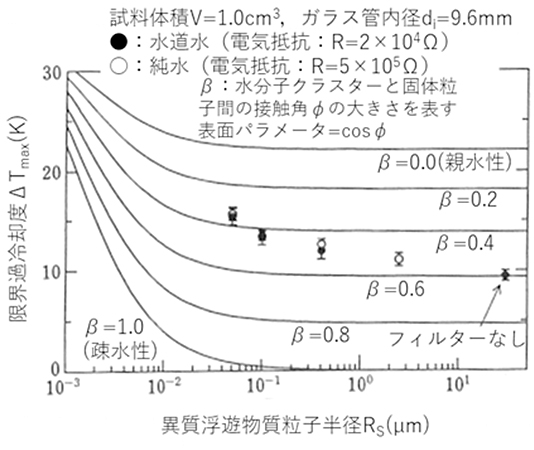
図11 異質粒子半径\(R_s\)と限界過冷却度\(ΔT_{ max }\)の関係
写真3は、直径50mmのガラス製シャーレ内に充填された水道水(体積5cm3)に、不均質氷核生成物質としてヨウ化銀を混入した場合の過冷却状態解消時の様子をシャーレ底面より撮影したものです。過冷却水の凍結は、シャーレ底部に沈澱したヨウ化銀粒子表面より発生しており、ヨウ化銀粒子を中心として放射状に樹枝状氷結晶が成長している様子が観察されます。この氷結晶成長より、過冷却水の氷核生成がヨウ化銀表面にて起こり、不均質氷核生成位置を中心として氷結晶が順次水相へ成長していることが分かります。
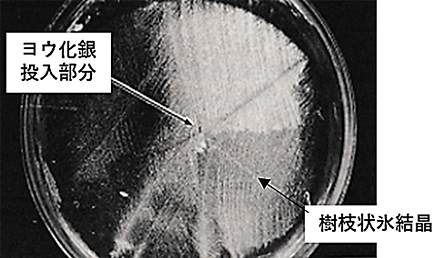
写真3 氷核生成物質を含む水の凍結挙動
図12は、様々な氷核生成物質を含む水道水にて、不均質氷核の限界過冷却度\(ΔT_{ max }\)に及ぼす効果を実験により示したものです。実験結果は、蒸留水とコレステロールが最も大きな氷核生成作用を有していることが分かります。限界過冷却度\(ΔT_{ max }\)の低下量は、およそ0~5K程度と蒸留水の場合の5~15Kであり、比較的小さなものとなっています。また、ヨウ化銀および硫化銅を混入した水道水の限界過冷却度の低下量は、最大でも2K程度です。このことから、基準となる水の特性が、氷核生成物質を混入した場合の限界過冷却度に対しても影響を及ぼしており、さらに、水道水のような予め多くの不純物質を含んだ水の場合には、これら含有不純物質と氷核生成物質の相互作用の程度により、限界過冷却度の低下割合が大きく変化することが予測されます。
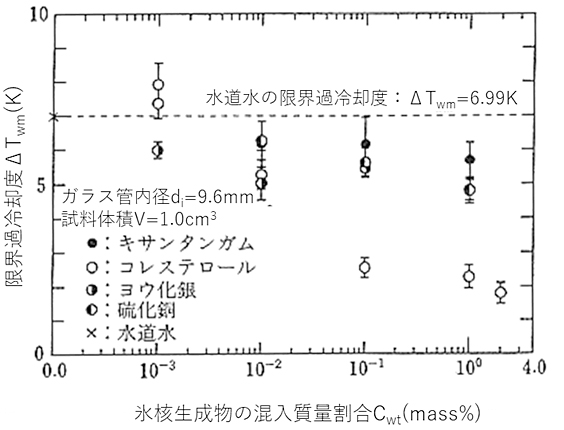
図12 限界過冷却度に及ぼす氷核生成物質の混入質量割合の影響(水道水)
水に他の溶質(無機物質や有機物質)を混合すると混合物の凝固点降下が起こることは、例えば融雪剤などの利用で、よく知られています。
薄い水溶液の凝固点降下度\(ΔT_f(=T_e-T_f)\)は、一定量の溶媒(水など)に溶けている溶質の分子数(モル濃度)に比例し、溶質の種類には関係しないことになり、以下の関係式で表せます(ラウールの法則)。図13は、温度と水蒸気圧の関係で、凝固点降下を示したものです。
\(∆T_f=1.88×C_{m}\)
ここで、\(C_{m}\):溶質のモル濃度です。
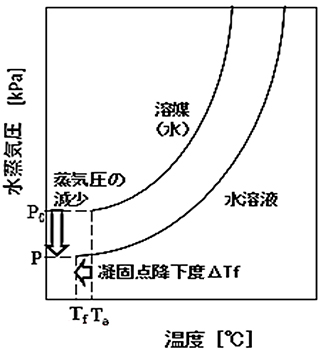
図13 温度と水蒸気圧(凝固点降下)
水溶液の凍結は、凝固点降下や構成的過冷却など水溶液の濃度に起因する現象や、固液共存の不均質凍結層の生成など、多成分系物質の凝固に特有な性質を有しています。さらに、これらが溶質の種類によっても異なることから、水のような純物質の凍結とは大きく異なる挙動を示します。写真4は、塩化マグネシウム水溶液を徐冷した場合に生成した結晶構造を示しています。写真4の白色部が氷結晶で、黒色部は水溶液相です。白色部分の氷結晶は、かゆ状氷結晶(mushy ice crystal) と呼ばれており、氷結晶に方向性を伴わない等軸結晶構造が発生している様子が分かります。
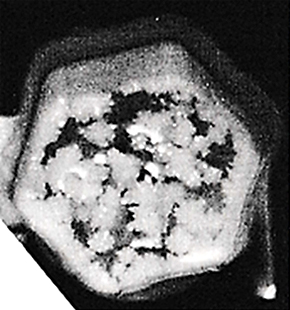
写真4 塩化マグネシウム水溶液の凝固状態
図14は、無機系溶液である塩化ナトリウム水溶液(質量濃度\(C_{ wt }=2\)%)を充填した矩形容器の側面から冷却・凝固させた場合における、冷却面近傍温度(図中黒丸印)および固液界面温度(図中白丸印)の経時変化を示しています。さらに、図14の上段には、生成される氷結晶の状態を模式的に示してあります。
塩化ナトリウム水溶液のような無機塩の共晶系水溶液の凝固過程は、以下に示す三つの過程より構成されます。
- ①初期過程:図14中のA点において、冷却面近傍より水溶液の過冷却状態が解消され、急速な樹枝状氷結晶が発生し、凝固潜熱の放出による冷却面近傍水溶液温度の急激な上昇傾向が観察されます(図14中のB点)。このように短時間での過冷却解消過程を経た後、冷却面近傍で発生した氷結晶は、図14中のC点までの間に稠密(ちゅうみつ)化した平坦な氷層へと変化します。
- ②緩和過程:固液界面前方では、排出された溶質成分による濃度が顕著に増加し、その濃度分布に依存する平衡凍結温度\(T_e\)より温度\(T\)が低くなると、組成的過冷却状態*2 (constitutional subcooling)となり熱力学的に不安定となります。固液界面近傍では、組成的過冷却状態の解消により、再び樹枝状の氷結晶が発生し、この樹枝状氷結晶間に高濃度の水溶液を抱き込んだ固液共存域が成長し、最終的には固液平衡状態へと緩和されます。
- ③定常過程:さらに緩和過程が進行すると、固液共存域が完全な混合状態となり、固液共存域の先端温度(図14中の白丸印)が、初期濃度に対する平衡凍結温度となります。ただし、固相と共存相の境界位置は、共晶温度に達するまで停滞します。共晶系水溶液の凝固挙動は、温度分布や溶質成分の液相への排出に伴う濃度分布に依存した3種類の凝固過程を経て進行し、生成される氷結晶の性状は、凝固過程に依存することになります。
*2 組成的過冷却:水溶液の凝固に伴って、溶質の再分布によって生じる過冷却のことです。
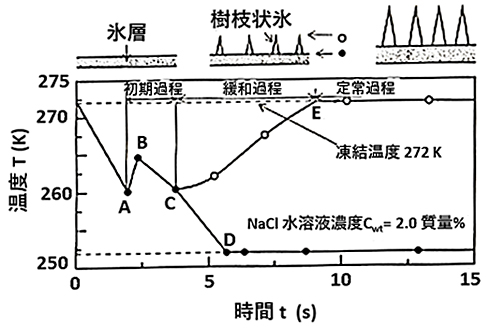
図14 凍結過程における温度の経時変化
一方、有機水溶液であるエチレングリコール水溶液の凍結層性状は、初期濃度および冷却条件により3種類に分類されます。まず初期濃度および冷却熱流速度が共に小さい場合には、冷却面に対して斜め方向に針状氷結晶が形成される斜方針状氷結晶領域となります。さらに、初期濃度および冷却熱流速度がともに大きな場合には白色不透明な凍結層領域となります。また、これらの中間的存在として冷却面と垂直な針状氷により構成された凍結層の領域となります。
組成的過冷却が起こると、平滑な凍結界面から、セル状界面に移行します。これは、図15に示すように、平滑な凍結界面に微小突起状に氷層が成長すると、その先端部ではさらに突起の成長がみられます。その結果、突起の両端P部は、排出された溶質の増加に伴う氷点降下より、氷の融解が起こり、この部分が、図15に示すように窪むことになります。結果として、図15の右側に示すセル状の組織が現れ、A-A断面のような網目模様の凍結界面となります。
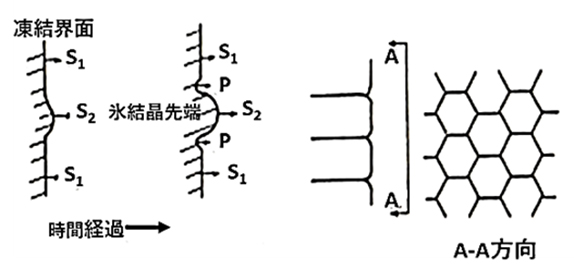
図15 有機水溶液の組成的過冷却に基づく氷界面の挙動
凍結界面近傍の水溶液は、図16に示すように、組成的過冷却に通常の過冷却が加わることになります。この状態では、凍結界面前方に進むほど過冷却が増大し、樹枝状氷結晶が発生することになります。また、この過冷却が極端に大きくなると、熱拡散が物質拡散を大きく上回り、熱拡散領域となり、濃度変化の伴わない無拡散凍結となり、凍結組織は粒状化すると言われています。
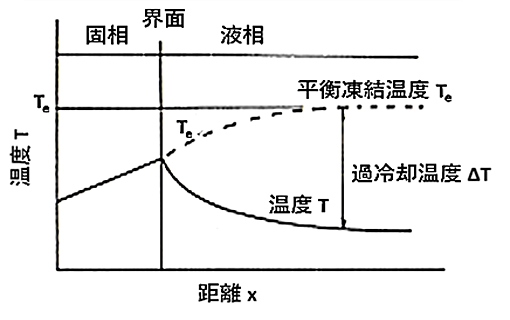
図16 有機水溶液の凍結を伴う固相と液相の温度分布
図17は、有機および無機水溶液における質量モル濃度 \(C_{ mol }\)と過冷却度 \(ΔT_e\)の関係を示しています。有機水溶液の\(ΔT_e\)の値は、高濃度域で若干上昇する傾向にあるものの、\(C_{ mol }\)に依存せずにほぼ \(ΔT_e≒0\)であり、ラウールの法則とよく一致した凝固点降下度\(ΔT_{ fs }\)を有しています。一方、無機水溶液の場合は、比較的低濃度域から\(ΔT_e\)の増加がみられ、さらに\(C_{ mol }\)の増加とともに急激に増加している様子が分かります。
無機水溶液の凝固点降下度\(T_{ fs }\)は、モル凝固点降下度 \(ΔT_{ mol }\)から大きく逸脱しており、水溶液中の溶質成分が比較的強く水分子に影響を与えているものと推察されます。
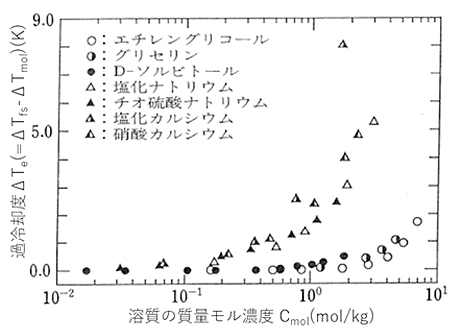
図17 溶質の質量モル濃度\(C_{ mol }\)と過冷却度\(ΔT_e\)の関係
水溶液の凍結に関して、凝固点降下や組成的過冷却、溶液の濃度に起因する現象そして固液共存の不均質凍結層の生成などの特徴があり、それらは溶質の種類によっても異なることになります。
写真5は、透明容器にエチレングリコール水溶液を入れ、底面を冷却した場合に得られる凍結層の性状を示しています。写真5の下段には、実験条件である初期濃度\(C_{0}\)、初期温度\(θ_{w}\)、冷却面温度\(θ_{\infty}\)の値を示しています。一般に、写真5(a)に示す樹枝状氷または針状氷(dendritic ice)が生成します。樹枝状凍結層が形成される理由としては、凍結の進行に伴って凍結層界面に溶質が析出され、凍結層界面近傍に濃度分布が生ずることにより起こる組成的過冷却と呼ばれる過冷却現象により、界面に不安定性が発生するためです。
また、写真5(b)に示す濃度が高くかつ冷却面温度が平衡凍結温度(\(θ_{e}\):濃度により変化)よりも十分に低い場合には、白色不透明の凍結層が生成します。
強制対流下に置かれた冷却水平円柱周りのエチレングリコール水溶液(濃度5%)の凍結状態を写真6に示します。写真6(a)の主流速度が\(U_{\infty}=0\)m/sの場合、針状凍結層がほぼ半径方向に成長していますが、側面から下方向に析出した溶質が凍結層表面に沿って流下するため融解が生じ、縞模様が形成されています。さらに主流速度が大きくなるに従って、流れの剥離点近傍に形成されるステップが上流方向(写真では左側)へ移動します。そして、写真6(d)に示す\(U_{\infty}=0.07\)m/sの場合には、真円に近い形状で表面は滑らかな状態でステップが認められなくなります。

写真6 冷却円筒の周りの水溶液が流動する場合の凍結層の状態
水の過冷却解消には、上述の水分子クラスターからの均質氷核生成とヨウ化銀で代表される不均質氷核生成があります。一方、水の結晶化を阻害する物質を利用することで過冷却を促進または安定させることができます。
過冷却促進に関連しては、越冬昆虫の血液中にはグリセロールやトレハロースなどのポリヒドロキシ化合物が高濃度で含まれていることが多いとされています。これらの物質は氷よりも液体の水の構造と適合しやすく、過冷却状態を促進安定する効果を有しています。さらに、寒冷地の樹木においては、-40℃まで過冷却して越冬する細胞に過冷却を促進させるフラボノイド配糖体やタンニンが存在することが明らかにされています2)。
一方、過冷却安定に関連しては、極海に棲む魚の体液中には凍結抑制タンパク質が含まれており、海水温度(~-1.5℃)でも過冷却を維持できます。このタンパク質の親水性部分が氷結晶のプリズム面(a軸方向)に吸着されると、氷結晶の成長は、図18に示すように氷結晶面積の増大をもたらします。すなわち、不凍タンパク質AFP(AFP:
Anti-Freezing Protein)が付着した場所と氷結晶との境界線の間における水素結合状態の変化により、近隣の過冷却水分子が氷結晶に組み込まれることが阻害されて過冷却状態が安定すると報告されています3)。このような過冷却安定機能を有する物質は、キノコなど植物類からも多数発見されています。このような過冷却安定物質は、不凍タンパク質として、食品分野を始めとして様々な産業で利活用されています。
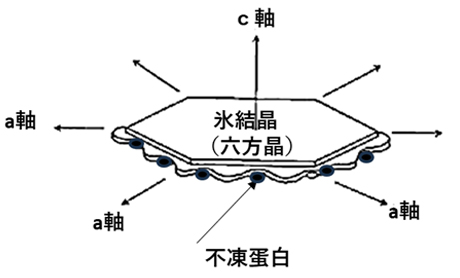
図18 不凍タンパク質による凍結抑制のメカニズム
(2)過冷却現象の利用技術
上述の水および水溶液の過冷却現象を利用した技術を以下に紹介します。
(a)流動する水および水溶液の過冷却を利用した氷蓄熱
第14回氷蓄熱の基礎と種類においては、様々な氷蓄熱の種類を述べています。ここでは、流動する水や水溶液の過冷却状態から氷スラリーの製造方法について説明します。
図19は、外管をブラインなどで冷却している二重円管熱交換器の内管に水や水溶液を流すことで過冷却状態を形成し、管外へ流出した過冷却水や水溶液を衝突板や超音波などの外部刺激を与えることで、過冷却状態を解消して流動性に富む氷スラリーを製造する方法の概要を示しています。この過冷却製氷システムでは、以下に同熱交換器内で水や水溶液の過冷却状態を安定維持するかが重要なポイントとなります。従って、同熱交換器内管に、氷結晶が混入しないようにフィルターそして最適な過冷却度を得るための温度調整用ヒーターを設けています。
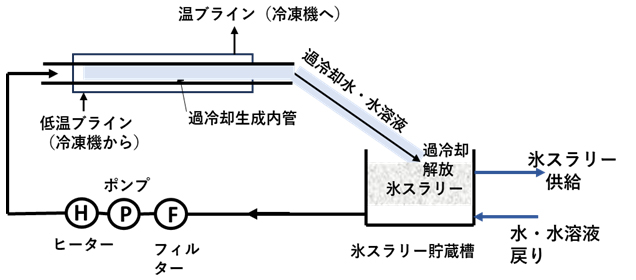
図19 流動過冷却水や水溶液による氷スラリー製造装置の概要
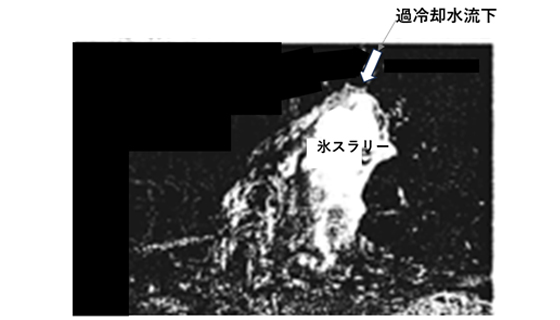
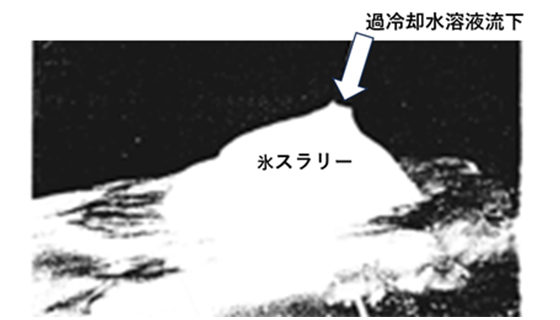
同氷スラリー製造装置により、生成した過冷却水および過冷却水溶液氷スラリーの状態を示したものが写真7です。まず、写真7(a)は、過冷却水の過冷却度が大きな場合の氷スラリーの状態を示したもので、シャーベット状の氷結晶となります。また、過冷却度が比較的小さい場合には、同内管出口から排出した過冷却水は衝突板により生成した氷は流下する過冷却水方向に成長して、所謂逆つらら状態となり、最終的には同円管内過冷却水は氷による閉塞状態となります。一方、過冷却水溶液(D-ソルビトール水溶液)の場合には、写真7(b)に示すように、柔らかい微細氷結晶を伴う氷スラリーとなります4)。
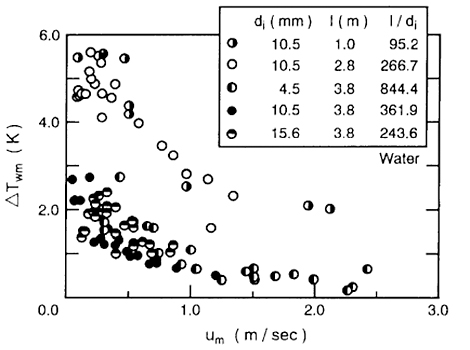
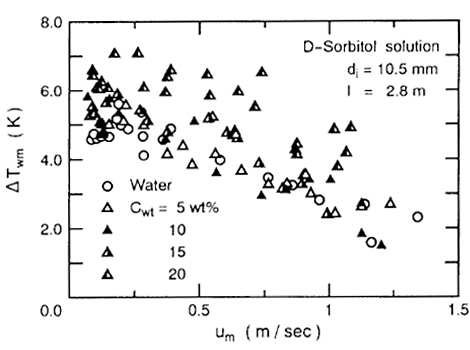
図20は、流動する過冷却水(a)およびD-ソルビトール水溶液(b)の管内流速\(U_m\)(m/s)と過冷却度\(ΔT_{ wm }\)(℃)の関係を示したものです。
水の場合については、同二重管式熱交換器内管の直径\(d_i=4.5\)mm~\(15.6\)mmそして管長\(ℓ=1.0\)m~\(3.8\)mとしています。D-ソルビトール水溶液の場合は、直径\(d_i=10.5\)mmそして管長\(ℓ=2.8\)mとしています。また、\(過冷却度ΔT_{ wm }=凍結温度T_f-冷却温度T\)としています。水の場合は、\(T_f=0\)℃として水溶液の場合の\(T_f\) は、水溶液濃度による凍結温度としています。
水およびD-ソルビトール水溶液の場合は、いずれも、流速の増加と共に、過冷却度の減少傾向があることが分かります。さらに、D-ソルビトール水溶液の過冷却度の方が、水の場合よりも過冷却度が大きくなる傾向にあることも分かります。
図21は、清水(せいすい)をプレート型熱交換器にて過冷却状態を生成する場合の冷却システム系統を示したものです。製氷槽に過冷却解除板を設けています。同熱交換器の流動する過冷却水への氷結晶の流入を防止するために、目の細かいフィルターや予熱器で温度調整がなされています。図21は、清水の過冷却水状態の生成状態の経時変化を示したものです。過冷却度が1.8℃に達する様子が理解できます。写真8は、過冷却水が解除板により、氷スラリーが生成される様子を示したものです5)。
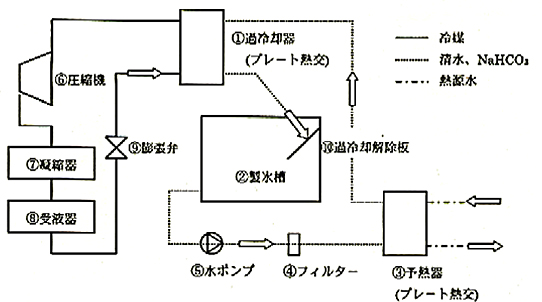
図21 過冷却水製造にプレート式熱交換器を利用した場合の製氷システム系統図
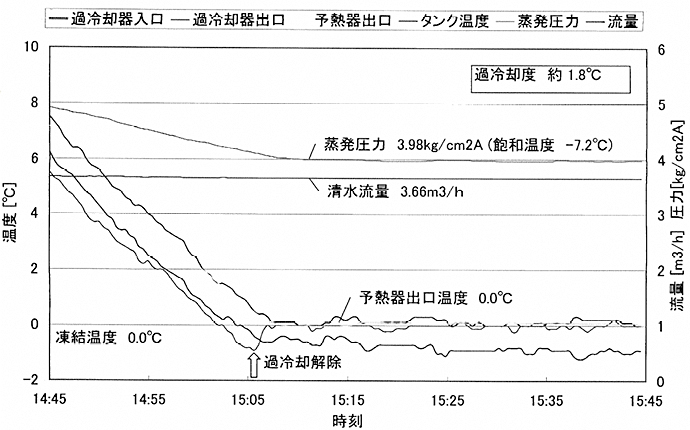
図22 清水の過冷却度1.8℃の場合の各部分温度の経時変化

写真8 過冷却水の衝突板による氷スラリー生成の様子
(b) 加圧による凍結温度の低下を利用する技術
水を加圧すると凍結温度が低下し、その凍結温度以下に冷却すると過冷却状態になり、圧力を除くと氷結晶を生成することになります。図23は、蒸留水に圧力を加えた場合の圧力と凍結温度の関係を示したもので、196MPaでは凍結温度は-20.2℃に低下します。
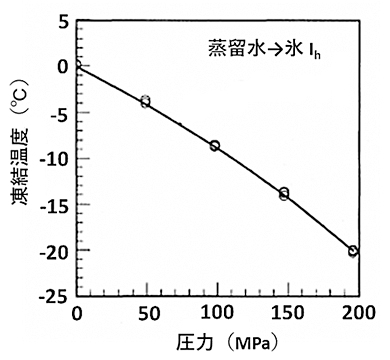
図23 圧力と凍結温度の関係
加圧による凍結温度低下現象を食品の加エプロセスへ応用することが提案されています。例えば、高圧下で食品を未凍結のまま0℃よりかなり低い温度で保存する加圧不凍結貯蔵は、食品を解凍する際に加圧することで凍結点を下げ周囲の熱媒体との温度差を大きくして急速に解凍する加圧解凍、さらに、食品を高圧下で凍結しない程度に冷却した状態から急激に復圧して急速凍結する圧力移動凍結法などがあります。
写真9は、卵液ゲルを-20℃の状態で、印加圧力を種々に変えて凍結し、その後室温で解凍した場合の卵組織の顕微鏡写真です6)。写真の灰色に見える部分は、卵の細胞組織で、黒く見える部分は氷結晶が融解した後の空隙です。
大気圧状態の写真(a)から500MPaの写真(c)へと圧力の増加と共に、氷結晶の大きさが小さくなっている様子が分かります。このように得られた微細な氷結晶の凍結卵を解凍すると水分の漏液(ドリップ)を伴わない凍結前の卵の状態が得られます。
(c)人工降雨や降雪における過冷却解消
大気温度は、100m上がるごとに約0.5℃降下します。上空3,000m以上では、気温は、-15℃以下となります。このような上空での雲は、過冷却状態にある微細な水滴群から構成されています。過冷却状態の水滴直径は、数µm~数十µm程度で光が当たると散乱して白く見えます。このような微細な過冷却状態の水滴群である雲の中へ、飛行機や対空砲などで、ヨウ化銀やドライアイスなどの氷核生成物質を散布すること(クラウドシーディング)で、氷結晶群(雪)を生成させます(図24)。様々な大きさを有する微細な氷結晶群のなかでは、小さな氷結晶は水蒸気圧が多大きいために昇華蒸発して大きな氷結晶へ昇華凝結して大きな氷結晶となり降下します。地上付近の気温や湿度に応じて、降雪や降雨となります7)。
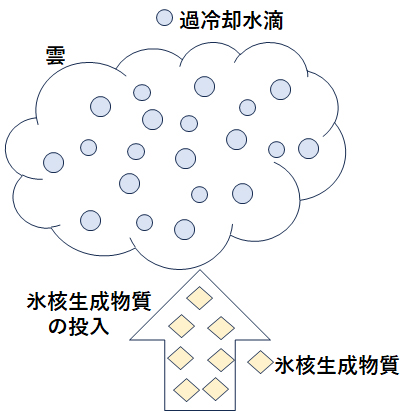
図24 雲の状態と氷核生成物質の投入
人工降雪機(写真10)は、低温の大気中に水を噴霧することで人工的に雪を作り、積雪を生じさせるための装置です。圧縮空気の噴射で散雪を行うガンタイプ(スノーガン)、大型のファンを用いるファンタイプ(スノーマシン)があります。
人工降雪機の原理は、水と圧縮空気を混合したものをノズルから噴射すると、水は激しい気流によって細かい水滴になるとともに、圧縮空気の断熱膨張により冷却されて過冷却水滴になります。噴射された微細な水滴は機械的衝撃や添加した氷核生成物質の作用で凍結を起こし、氷粒子を生成します。人工降雪機による雪片は水滴と同じく球形に近いために、自然雪に比べて粒子表面積が小さく解けにくい、雪質に粘りがなくサラサラしている特徴があります。代表的な氷核生成物質として氷核活性タンパク質や無機鉱物などがあります。これらの物質の分子構造は氷結晶と類似しているため、その表面に凝集した水分子のクラスターは固体の氷と同じ配列を取りやすくなります。氷核活性タンパク質は知られている物質の中で特に高い氷核活性を持ち、氷核活性を有する氷核活性細菌の一種であるシュードモナス・シリンガエ(ライラック樹木から取り出した極鞭毛を持つグラム陰性桿菌:細長い棒状の細菌)の乾燥菌体が商品化され、人工降雪用の核化剤として広く用いられています。

Snowmaking-mount-hotham,Wongm,2008,CC BY-SA 3.0
写真10 人工降雪機の造雪風景
図25は、人工造雪可能な気温と湿度の関係を示したものです。大気条件が赤線の曲線より下であれば造雪が可能です。造雪には一般に湿度が高いほど、より低温であることが必要です。また、気温が0℃そして低湿条件においては、噴射した微細水滴の蒸発により、周囲気温が氷点下となることで造雪が可能となります。
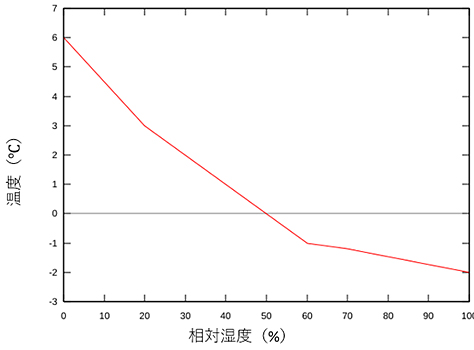
Snow Making Curve,Grendelkhan,2006,CC BY-SA
3.0
図25 人工造雪可能な気温と湿度の関係
(d) 過冷却現象を利用した微細氷結晶を伴う飲料
水やジュースなどの水溶液を冷凍庫内で冷却することで、発生する過冷却現象を利用したシャーベット状やスラリー状の氷結晶を伴う低温飲料です。写真11は、容器入りの日本酒を冷凍庫で冷却して、コップに注ぐ衝撃で過冷却状態の解消を行い、柔らかいシャーベット状の氷結晶を生成させてものです8)。柔らかい氷結晶を含む食感の日本酒を味わうことが出来ます。最近は、夏場に容器入りスポーツドリンクを冷却して過冷却状態を生成後に、容器に機械的刺激を与えることで、シャーベット状の柔らかい氷結晶を含む低温飲料として展開が進みつつあります。
過冷却状態の解消で、シャーベット状の氷結晶の生成メカニズムは以下のようです。
上述の図14において説明したように、有機水溶液の凍結過程で見られる組成的過冷却によるものです。まず、ジュースなどの有機水溶液は、冷却温度の低下とともにまず、熱的過冷却状態(温度変化)の解消が行われて、微細な氷結晶が現れます。氷結晶の周囲は有機水溶液の濃度が増加して、その水溶液の凝固点が低下して、組成的な過冷却領域となります。その後、組成的な過冷却が解消されるとシャーベット状の比較的柔らかい氷結晶が生成することになります。組成的過冷却度が大きいほど微細な柔らかい氷結晶となります。組成的過冷却度は、冷却速度や有機物の種類などで変わります。
このように、有機物の種類や濃度により過冷却度が変化することなり、生成する氷結晶の構造や大きさなども変化することになります。

写真11 過冷却した冷酒をコップに注ぐことで過冷却解消後に生成したシャーベット状氷結晶の様子
(e)過冷却現象を利用した食品の保存
野菜や果物などの食品を過冷却状態の形成後に凍結を進行させた場合に得られる凍結食品の品質向上に関する報告があります。過冷却状態により凍結させた場合には、過冷却度の増加とともに氷結晶の大きさは小さくなり、解凍後のドリップ(液汁)の排出は少なります。写真12は、豆腐を通常の凍結状態の場合と過冷却を-7℃の状態から凍結を行い、-5℃で1ヶ月保存して、再結晶化した場合のX線CT画像を示したものです。過冷却を伴わないで凍結した豆腐は氷結晶の粗大化がみられ、さらに氷結晶の分布も不均一となります。一方、過冷却後の凍結においては氷結晶の粗大化は見られず、結晶の分布も大きな偏りはない結果となります。このように含水食品の凍結に過冷却現象の利用は食品の凍結保存に良好な結果をもたらすことになります9)。一方、ナシやブドウそしてチューリップなどでは、凍結させないで-2℃の過冷却状態での保存が実施されています。
(f)氷衣掛けによる過冷却回避による果樹などの凍結防止
果樹などは春先の発芽期以降は、生育ステージが進行するにつれて耐凍性が低下することになります。果樹などが放射冷却や寒波により、果樹などの周囲水分が過冷却状態を経て凍結が進行する霜害が発生します。このような霜害を回避する方法の一つに、散水氷結法(氷衣掛け法)があります。散水氷結法は、スプリンクラー等からの散水により作物体に用水を付着させ、その水が氷結する際に放出する潜熱を利用して、凍結温度(0℃)付近を保持し、気温の低下から果樹の芽などを保護する方法です。写真13は、リンゴ樹枝に散水し、結氷させた状態で、氷衣掛けで果樹などを霜害から回避しています。散水から氷への相変化による潜熱放出を利用するために、連続的な散水が必要となります10)。

写真13 リンゴ樹枝に散水して結氷した状態
(g)アイスクリーム製造時フリージング過程における過冷却現象の利用
写真14に示すアイスクリームは、原料(乳脂肪分、糖類、乳化剤、安定剤、水分)を混合、均質化、殺菌、冷却、エイジングそしてフリージングなどの過程を経て製造されます。
アイスクリームのフリージングは、アイスクリーム原料と空気を混合(オーバーラン)させながら冷却させると、含有している微小水滴の過冷却状態より、急速に微細な氷結晶が形成されます。冷却速度の調整により、過冷却度が大きければ大きいほど氷結晶が緻密となり、まろやかな良質のアイスクリームになると言われています11)。

写真14 アイスクリームの外観
参考文献
- 1)稲葉英男、福迫尚一郎、低温環境下の伝熱現象とその応用、㈱養賢堂発行(1996)、頁81
- 2)藤川清三、過冷却促進物質、日本機械学会誌、119巻3号、頁161
- 3)村勢則郎、水の低温物理化学と生物、日本食品工業学会誌、41巻9号(1994)、頁646
- 4)稲葉英男、武谷健吾、流動過冷却水および管内凍結発生限界に及ぼす諸因子の影響、日本機械学会論文集(1994)、第60巻578号、頁3440
- 5)深村真史ら、過冷却製氷方式に関する研究、(株)前川製作所報告書(1999)、頁2
- 6)渕上倫子ら、圧力移動凍結した食品の物性と微細構造、圧力の科学と技術(2008)、18巻2号、頁133
- 7)折笠成宏ら、航空機を用いた雲へのシーディングによる人工降雨・降雪実験(2015)、エアゾル研究第30巻1号、頁24
- 8)(株)MARS Company、カタログ:マイナス7℃でも凍らない、Tokyo Snowman Super Cooling System
- 9)君塚道史、小林りか、食品冷凍への過冷却利用とその効果、日本水産学会誌(2016),第82巻6号、頁967
- 10)安達栄介、果樹凍霜害対策マニアルの概要および今後の対策推進について、山形県農林水産部果樹凍霜害対策研修会資料(2022年)、頁16
- 11)則竹寛子ら、アイスクリームの保存温度の変動による氷結晶形態の変化、日本冷凍空調学会(2012)、第29巻2号、頁263